
Strategie Ventilatorie nel Neonato
Dott.
Gianfranco Maffei
Dirigente Medico U.O. di Terapia Intensiva Neonatale, Policlinico di Foggia,
Italy
Vol. 2, N. 3, Maggio 2004
Nel neonato la ventilazione meccanica è solitamente una misura temporanea di supporto alla funzione polmonare fino al raggiungimento di una completa autonomia ventilatoria.
I suoi obiettivi sono:
- provvedere ad una adeguata ventilazione alveolare con rimozione della CO 2 e ad una soddisfacente ossigenazione;
- ridurre il lavoro respiratorio.
In considerazione dell'eziologia multifattoriale del danno polmonare cronico, in cui il supporto ventilatorio svolge ancor oggi un ruolo di rilevante importanza, ben si comprende come una strategia ventilatoria in grado di soddisfare nel miglior modo possibile agli scambi gassosi senza peraltro arrecare particolare danno al polmone ventilato, rappresenta l'aspettativa cui ogni intensivista dovrebbe protendere.
FISIOPATOLOGIA RESPIRATORIA
L'elevato metabolismo, la riduzione della Capacità Funzionale Residua e della Compliance Polmonare, l'incremento delle resistenze al flusso aereo ovvero la presenza di shunts dx-sn (dotto di Botallo, forame ovale) rendono ragione del facile deterioramento degli scambi gassosi cui i neonati ed ancor più i prematuri sono esposti.
Ipossiemia
L'ipossiemia, ovvero una bassa tensione di O 2 nel sangue solitamente arterioso può essere la conseguenza di almeno 4 condizioni:
• Ipoventilazione
• Alterazioni della diffusione attraverso la membrana alveolo-capillare
• Shunt destro-sinistro intra-extracardiaco
• Disomogeneità del rapporto ventilo/perfusorio (mismatch V/Q)
Nell'ipoventilazione pura, solitamente la PaO 2 solitamente non scende mai a livelli molto bassi e si accompagna sempre ad un aumento della PaCO 2 . In questa condizione come nelle alterazioni della diffusione attraverso la membrana alveolo-capillare, l'ipossiemia è facilmente corretta da un aumento della frazione di ossigeno nell'aria inspirata. La stessa cosa non accade nel caso trattasi di uno shunt dx-sn, nel cui caso peraltro la PaCO 2 si presenta spesso ridotta come conseguenza di uno stato d'iperventilazione secondario all'ipossiemia stessa. Nel neonato con insufficienza respiratoria da RDS il mismatch V/Q rappresenta senza dubbio la causa più importante di ipossiemia.
In corso di ventilazione meccanica convenzionale, l'ossigenazione è determinata largamente dalla frazione di ossigeno inspirato (FiO 2 ) e dalla Pressione Media delle vie Aeree (MAP) durante il ciclo ventilatorio, che può essere calcolata attraverso l'equazione di Boros:
MAP = K (PIP-PEEP) Ti/Ti+Te + PEEP |
La costante (K) presente nella formula, è determinata dalla velocità del flusso e dalla velocità d'innalzamento della curva pressoria. Quest'equazione indica che la MAP aumenta con incrementi della PIP, PEEP, del rapporto Ti/Ti+Te, e del flusso (che a sua volta incrementa K attraverso la creazione di una curva più quadrata).
L'incremento della MAP migliora l'ossigenazione attraverso l'aumento del volume polmonare ed il miglioramento del rapporto V/Q. Esiste, quindi, una stretta correlazione tra MAP ed ossigenazione. Tuttavia una MAP troppo elevata può causare sovradistensione degli alveoli, portando ad uno shunt destro-sinistro del sangue a livello polmonare oltrechè essere trasmessa alle strutture toraciche, specie alla presenza di un polmone con una compliance normale, con riduzione dell'output cardiaco.
Ipercapnia
L'ipercapnia, ovvero l'aumento delle pressioni parziali del gas carbonico al di sopra dei valori di equilibrio, è solitamente causata da
• Ipoventilazione
• Alterazioni del rapporto ventilo/perfusorio.
L'ipercapnia acuta raramente è pura, essendo il più delle volte associata ad una condizione di ipossiemia. L'eliminazione della CO 2 è direttamente proporzionale alla ventilazione alveolare minuto, la quale a sua volta è determinata dal prodotto tra volume alveolare (volume corrente meno la ventilazione dello spazio morto) e la frequenza. Così la ventilazione alveolare minuto è calcolata come segue:
Ventilazione
alveolare minuto= (volume corrente - spazio morto) x frequenza |
Aumentando o il volume corrente o la frequenza, aumenta la ventilazione alveolare con riduzione della pressione parziale arteriosa del gas carbonico. Poiché la ventilazione dello spazio morto è pressoché costante, le variazioni nel volume corrente appaiono più efficaci nel modificare l'eliminazione della CO 2 rispetto alle semplici variazioni della frequenza. Pur tuttavia in neonatologia bisogna tener presente che volumi correnti elevati possono arrecare danni alle strutture polmonari (baro-volutrauma) e per tal motivo è preferito l'impiego di volumi relativamente piccoli e frequenze solitamente elevate.
MECCANICA POLMONARE
Le interazioni tra ventilatore e neonato dipendono strettamente dalle proprietà meccaniche del sistema respiratorio.
L'esistenza di un gradiente pressorio, per un tempo adeguato, tra l'apertura delle vie aeree e gli alveoli è in grado di generare un flusso gassoso in-espiratorio.
Utilizzando un modello di tipo monocompartimentale, costituito da un tubo di conduzione (T) e da un contenitore elastico (C), che simuli le vie aeree ed il recoil elastico della parete toracica e dei tessuti alveolari, appare ovvio che tale pressione d'inspirazione dovrà essere in grado di vincere la resistenza delle vie aeree al flusso inspiratorio e quelle legate al recoil elastico stesso ( Forze Elastiche e Forze Resistive del polmone).
Fig.1
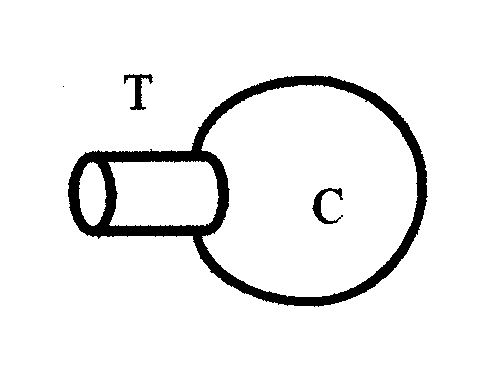 |
Limitando l'osservazione alla camera elastica (C), per ogni variazione di pressione seguirà una variazione di volume, cioè del gas fluirà all'interno della camera.
Il rapporto tra questi due parametri esprime la Compliance secondo la formula:
C = rV/ r P |
Purtroppo in vivo, questo parametro non è costante al di fuori di un limitato range di volume che corrisponde approssimativamente al volume corrente (Vt).
Infatti, a volumi bassi, vicini alla Capacità Funzionale Residua (CFR) ovvero molto alti prossimi alla Capacità Polmonare Totale (CPT), essa Compliance decresce.
Da quanto detto è possibile affermare che se vogliamo erogare un adeguato Vt, mantenendo una pressione inspiratoria sufficientemente bassa è indispensabile operare dentro la porzione centrale della curva della Compliance, evitando altresì la comparsa di aree atelettasiche o una sovradistensione polmonare.
Il range della Compliance totale del sistema respiratorio (polmone + parete toracica) nel neonato sano è 0,003-0,006 L/cm H2O, mentre la Compliance in neonati con RDS può essere molto bassa 0,0005-0,001L/cm H2O.
Nel modello in esame il tubo conduttore (T), rappresenta la resistenza delle vie aeree e dei tessuti al flusso gassoso.
Il rapporto matematico fra pressione e flusso esprime appunto una Resistenza secondo la formula:
R = r P/ r Fl |
Associando ora questi i due concetti su esposti (Compliance e Resistenze) è intuibile che la pressione necessaria per un'inspirazione è uguale alla somma delle due pressioni in esame, quella per vincere il recoil elastico e quella per contrastare le resistenze al flusso secondo la formula conosciuta come Equazione di moto del Sistema Respiratorio:
P insp. = V/C
+ (R x Fl) |
dove Compliance e Resistenze sono delle costanti determinate dalle caratteristiche proprie del paziente in un determinato momento, mentre il Flusso ed il Volume rappresentano delle variabili. Il range di Resistenze delle vie aeree più le resistenze respiratorie tessutali, nei neonati sani è 20- 40 cm H 2 O/L/s; nel neonato intubato questo range sale a 50- 100 cm H 2 O/L/s. Nell'ambito della meccanica polmonare, grande importanza ha il concetto di costante di tempo. Il ventilatore all'inizio del ciclo, causa una variazione istantanea di pressione nelle vie aeree, ma ovviamente occorrerà un certo tempo perché essa si equilibri con quell'esistente a livello alveolare.
Costruendo un grafico Pressione /Tempo o Flusso/Tempo otteniamo una curva di tipo esponenziale sia nell'inspirazione che nell'espirazione.
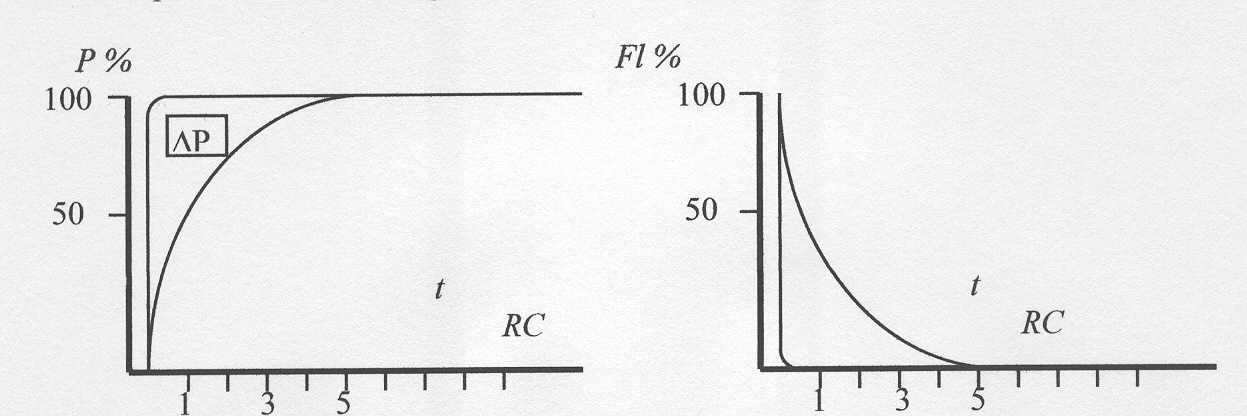 |
La forma di questa curva è determinata dai valori individuali di Compliance e di Resistenze per un dato paziente in un determinato momento.
L'aspetto più importante di tutto ciò è che qualunque sia la pressione inspiratoria utilizzata, solo dopo un tempo pari a 3 volte il valore del prodotto Compliance x Resistenze (Costante di tempo), si raggiungerà a livello alveolare, un valore pari al 95% della pressione utilizzata.
Analogamente nell'espirazione, dopo un tempo pari a 3 volte la Costante di tempo, la pressione alveolare sarà ridotta al 5%.
Pertanto come risvolto pratico abbiamo che il rispetto del valore della Costante di Tempo nella gestione del setting ventilatorio è importante per non avere uno spreco pressorio in fase inspiratoria o fenomeni d'air trapping al termine dell'espirazione.
Per esempio, il polmone di un neonato sano con una Compliance di 0,004 L/cm H 2 O ed una resistenza di 30 cm H 2 O/L/sec. avrà una costante di tempo di 0,12 secondi.
La più lunga durata del tempo d'inspirazione (o espirazione) permette per l'equilibrio, o una più alta percentuale di equilibrio. Ai fini pratici, un dato volume è rilasciato o una data pressione è trasmessa in maniera quasi completa (95-99%) dopo 3-5 volte la costante di tempo. Quindi la costante di tempo di 0,12 sec. calcolata per un neonato sano, indica la necessità di una fase inspiratoria o espiratoria di 0,36-0,6 sec. Al contrario, nei polmoni con ridotta compliance (es RDS) si avrà una costante di tempo più breve.
A complicare ancor più la situazione, vi è il fatto che la Compliance e le Resistenze delle vie aeree assumono valori differenti durante l'inspirazione e l'espirazione oltrechè variano in rapporto a differenti fasi della malattia di base ovvero possono assumere valori diversi per differenti regioni polmonari, come accade nelle malattie polmonari eterogenee (Displasia Broncopolmonare).
METODICHE DI VENTILAZIONE
Pressione positiva continua nelle vie aeree
La CPAP (Continuous Positive Airways Pressure) consiste nell'applicazione di una pressione positiva continua alle vie aeree del paziente in respiro spontaneo.
I suoi effetti benefici si attuano attraverso l'incremento del volume alveolare, il reclutamento e la stabilità alveolare e la ridistribuizione del liquido polmonare, ed in ultima analisi attraverso il miglioramento del rapporto V/Q. Comunque, alti livelli di CPAP possono associarsi ad effetti negativi.
La CPAP dà sicuri benefici nella RDS conclamata: ridotta richiesta di ossigeno, e ridotta necessità di ventilazione meccanica; al contrario se applicata profilatticamente nel neonato pretermine non sembra associarsi ad una ridotta incidenza o severità dell'RDS né tampoco sembra ridurre la frequenza delle complicanze o la mortalità.
La CPAP si è dimostrata in grado di:
• aumentare la CFR attraverso reclutamento di alveoli collassati permettendo di lavorare nella parte media della curva V/P con minor dispendio energetico;
• ridurre le resistenze nelle vie aeree in quanto stabilizza le stesse prevenendone il collasso;
• ridurre lo shunt intra-polmonare destro-sinistro grazie al miglioramento dell'ossigenazione ed alla vasodilatazione del piccolo circolo;
• stabilizzare la parete toracica riducendone il collasso inspiratorio ed abolendo altresì il riflesso inibitorio frenico-intercostale dell'inspirazione;
• rallentare la frequenza respiratoria per prolungamento del tempo espiratorio conseguenza dell'abolizione del riflesso di deflazione di Hering-Breuer;
• aumentare la pressione media nelle vie aeree (Mean Airways Pressure MAP) migliorando il rapporto ventilazione-perfusione;
• mantenere il surfattante sulla superficie degli alveoli;
• diminuire l'edema alveolare, ove fosse presente.
Fra gli effetti avversi correlati all'applicazione della CPAP bisogna segnalare un'aumentata incidenza di airleaks. E' una metodica molto impiegata anche nello svezzamento dalla ventilazione meccanica sia come momento unico e sia a seguire la ventilazione mandataria intermittente sincronizzata.
Ventilazione meccanica convenzionale
Introdotti in neonatologia intorno agli anni 70, i ventilatori pressione-limitata, tempo ciclati hanno avuto largo impiego; il settaggio è strettamente correlato ai valori emogasanalitici, alla meccanica respiratoria ed alla integrità o meno del drive ventilatorio.
Le variabili impostabili dal clinico, avendo come fine ultimo la ventilazione senza danneggiare il parenchima polmonare, sono:
PIP (Peak Inspiratory Pressure), pressione raggiunta la quale, avviene l'inversione del ciclo; l'elevazione della PIP aumenta il Volume corrente con riduzione della PaCO 2 , ed aumenta pure la MAP e la PaO 2 con esposizione, però, al rischio di baro-volutrauma ed airleaks. Il livello di PIP richiesta in un neonato, dipende grandemente dalla Compliance del suo sistema toraco-polmonare, in considerazione anche dei seguenti fattori quali peso del neonato, età gestazionale e postnatale, tipo e severità della malattia, concentrazione dell'ossigeno inspirato (indice indiretto della funzionalità polmonare), resistenze al flusso aereo. Un indicazione clinica di un'adeguata PIP è data dall'osservazione di un leggero innalzamento della gabbia toracica con gli atti mandatori meccanici e questo non dovrebbe essere mai superiore a quello che si realizzerebbe in respiro spontaneo. L'impiego della minor PIP efficace è sempre raccomandabile, tenendo sempre presente che questa è suscettibile di variazioni nel corso della evoluzione della malattia di base o allorquando siano adottate particolari misure terapeutiche come l'instillazione di surfattante esogeno.
PEEP (Positive End-Exspiration Pressure) pressione positiva di fine espirazione: condiziona la Capacità Funzionale Residua (CFR) e la MAP, favorendo entro certi limiti l'ossigenazione, con diminuzione però del Volume Corrente e quindi dell'eliminazione di CO 2 . PEEP particolarmente elevate (> 6 cm di H 2 O) inoltre influenzano la Compliance Polmonare , riducono la frequenza respiratoria spontanea del neonato ed ostacolare il ritorno venoso con riduzione dell'output cardiaco. Una minima PEEP è sempre raccomandabile in corso di ventilazione meccanica in quanto l'intubazione endotracheale elimina l'attivo mantenimento della CFR compiuto dall'adduzione delle corde vocali e dalla chiusura della glottide. (freno laringeo) Frequenza ventilatoria che nella ventilazione convenzionaleè ≤ 60 atti/min. Una frequenza elevata, incrementa la ventilazione minuto e quindi favorisce l'eliminazione del gas carbonico senza sostanziali influenze sulla PaO2. Oggigiorno sono preferite le strategie che impiegano frequenze elevate e volumi correnti ridotti, al fine di minimizzare il danno polmonare da sovradistensione. In quest'ottica, particolare attenzione va posta a non ridurre oltremodo il tempo espiratorio che potrebbe condurre ad un fenomeno di air trapping con riduzione della Compliance Polmonare.
Tempo Inspiratorio ed Espiratorio: gli effetti delle variazioni sui valori emogasanalitici sono influenzati dalla loro relazione con le rispettive costanti di tempo. Per quanto riguarda il tempo inspiratorio bisogna ricordare che se particolarmente lungo aumenta il rischio di pneumotorace, mentre è da preferire piuttosto corto (< 0,45 sec.) durante la fase di svezzamento per non favorire riflessi meccanici nel neonato.
Rapporto Inspirazione/Espirazione : da valori fisiologici di 1:2 può arrivare anche a valori di 1:1 (al di sopra del quale i benefici sono dubbi mentre è certo il baro-volutrauma e la diminuzione della gittata cardiaca) con miglioramento della PaO 2 attraverso un aumento della MAP.
Frazione di ossigeno inspirata (FiO 2 ): un suo aumento migliora in maniera intuibile l'ossigenazione alveolare. Ad un iniziale suo incremento al fine di ottenere un'adeguata ossigenazione, per via degli effetti tossici propri di questo gas medicale, fa seguito un aumento graduale della MAP rimanendo sempre entro margini di sicurezza, al fine di poter ridurre l'iniziale FiO 2 impostata. Durante la fase di weaning, invece, sempre per il rischio dei radicali liberi viene preferita un'iniziale riduzione della FiO 2 seguita in un secondo tempo da un abbassamento della MAP laddove le condizioni cliniche lo consentano.
Flow Rate compreso fra 6 e 12 l/m; l'impiego di flussi elevati permette di ottenere un'onda pressoria con morfologia quadrata e quindi aumento della PaO 2 oltre che della MAP; infatti nella formula da Boros per il calcolo della MAP la costante k è uguale a 0,5 se viene utilizzata un'onda a morfologia triangolare, mentre il valore si avvicina a 1 utilizzando un'onda a morfologia quadrata. Sono consigliati flussi elevati anche alla presenza di tempi inspiratori particolarmente brevi al fine di garantire un adeguato volume corrente.
Nell'ultimo decennio sono stati commercializzati nuovi sofisticati ventilatori in grado di migliorare l'outcome polmonare dei neonati ventilati e che consentono numerose modalità di assistenza ventilatoria.
Ventilazione paziente triggerata (A/C)
A differenza della ventilazione meccanica convenzionale (CMV) in cui è il ventilatore a controllare in toto la ventilazione del neonato, quella Assistita/Controllata prevede la possibilità di essere innescata dal paziente, offrendogli il comando della propria frequenza ventilatoria. La presenza di dispositivi trigger fa sì che sia lo sforzo del paziente a determinare l'inizio del ciclo ventilatorio. In assenza di un drive neuromuscolare integro, il ciclo ventilatorio verrà avviato da un dispositivo a tempo presente nel ventilatore.
Con un trigger di flusso, il neonato dovrà iniziare l'inspirazione onde creare un flusso di entità tale da superare il livello soglia preimpostato sul ventilatore, dopo di che verrà rilasciato un atto ad un settaggio predeterminato (PIP, tempo inspiratorio, flusso etc.). Se il neonato non riuscirà ad innescare un atto meccanico, la macchina funzionerà in CMV secondo una frequenza ventilatoria preimpostata. Jerreau P. et al. hanno dimostrato che la messa in fase della pressione negativa intratoracica con quella positiva generata dal ventilatore attuabile in corso di ventilazione A/C, comporta nel neonato un aumento del Volume corrente a cui si associa a una riduzione della frequenza ventilatoria con diminuzione del WOB rispetto ai neonati trattati con l'IMV (0,48 J/L vs 0,81 J/L) e durata della ventilazione meccanica.
Ventilazione mandatoria intermittente sincronizzata (SIMV)
A differenza della ventilazione A/C dove tutti gli atti compiuti dal neonato sono assistiti dalla macchina, nella SIMV solo alcuni di essi trovano assistenza meccanica.
Si tratta di una metodica che trova impiego soprattutto nello svezzamento del neonato dal ventilatore meccanico e le strategie attuabili a tal fine sono rappresentate da una riduzione del numero degli atti assistiti dalla macchina oltrechè da una riduzione della PIP o da una riduzione di sensibilità del trigger di flusso.
Ventilazione assistita proporzionale
Tranne il caso in cui esse siano flusso-ciclate, entrambe le modalità di ventilazione meccanica paziente-triggerata discusse sopra (PTV, SIMV) sono disegnate per sincronizzare solo l'inizio dello sforzo inspiratorio. In contrasto, la ventilazione assistita proporzionale (PAV) accoppia l'inizio con la durata del supporto inspiratorio ed espiratorio. Il supporto ventilatorio è in proporzione al volume e/o flusso del respiro spontaneo. Così, il ventilatore può selettivamente ridurre il lavoro elastico e/o resistivo del respiro. L'ampiezza del supporto può essere aggiustato in rapporto alle necessità del paziente. Quando paragonata alla Ventilazione convenzionale (CMV) ed alla PTV, la PAV riduce la pressione ventilatoria mentre migliora lo scambio di gas. Trias clinici randomizzati sono necessari per determinare se la PAV conduce a maggiori benefici quando comparata alla CMV.
Ventilazione ad alta frequenza
La ventilazione ad alta frequenza (HFV) può migliorare gli scambi dei gas perché, in aggiunta al trasporto dei gas per convenzione, altri meccanismi di scambi gassosi possono divenire attivi ad alte frequenze (profilo variabile della velocità dei gas durante l'inspirazione e l'espirazione, scambi gassosi tra unità polmonari parallele, incrementata turbolenza e diffusione). L'uso estensivo clinico delle varie forme di HFV è orami divenuto routinario in Terapia Intensiva Neonatale.
La ventilazione a pressione positiva ad alta frequenza usa ventilatori standard con tubi e connettori a bassa compliance, così che un adeguato volume corrente può essere rilasciato nonostante il tempo inspiratorio molto breve. La ventilazione jet ad alta frequenza (HFJV) è caratterizzata dal rilascio di gas da una sorgente ad alta pressione attraverso un iniettore. Il flusso di gas emesso dalla cannula produce un area di relativa pressione negativa che richiama gas dall'ambiente vicino. L'interruttore di flusso ad alta frequenza (HFFI) rilascia anche piccoli volumi correnti attraverso l'interruzione del flusso dalla sorgente di pressione, ma in contrasto con la ventilazione jet, l'HFFI non usa una cannula con iniettore. La ventilazione oscillatoria ad alta frequenza (HFOV) rilascia volumi molto piccoli (spesso più piccoli dello spazio morto) a frequenze estremamente elevate. La ventilazione oscillattoria è unica perché l'espirazione è generata attivamente, in contrapposizione ad altre forme di HFV, in cui l'espirazione è passiva.
STRATEGIE VENTILATORIE PARTICOLARI
Il danno polmonare legato alla ventilazione è correlato ad una serie di fattori quali le alte pressioni ventilatorie (barotrauma), gli alti volumi correnti (volutrauma) l'alta concentrazione d'ossigeno impiegata (danno ossidativi), l'eterogeneità del parenchima polmonare con predisposizione al baro-volutrauma delle zone più complianti, l'immaturità polmonare.
In quest'ottica oggi vengono adottate delle filosofie ventilatorie che prevedono l'impiego di volumi correnti relativamente piccoli e di contro valori di moderata ipercapnia rappresentano un prezzo sicuramente accettabile al fine di minimizzare o prevenire il danno polmonare ventilatore-indotto.
Così in un neonato con RDS, una strategia ventilatoria convenzionale ottimale potrebbe prevedere la più bassa PIP sufficiente ad erogare il volume corrente richiesto (4-6 ml/Kg), una modesta PEEP (3- 5 cm H 2 O), una ipercapnia permissiva (PaCO 2 45-60 mmHg). Chiaramente un programma di svezzamento ventilatorio precoce minimizza l'esposizione dei polmoni ai su menzionati fattori iatrogeni.
Displasia Broncopolmonare
La displasia broncopolmonare (BPD) rappresenta la sindrome polmonare cronica più frequentemente diagnosticata nei prematuri e si caratterizza con una eterogenea costante di tempo. Infatti le resistenze risultano spesso marcatamente aumentate. Una PEEP più elevata (4-6 cmH 2 O) è spesso consigliata in associazione a frequenza ventilatorie piuttosto basse ed aumentati tempi di in-espirazione. Al fine di evitare ulteriori danni polmonari in corso di ventilazione una moderata ipercapnia con acidosi respiratoria compensata viene spesso tollerata.
Ipertensione Polmonare Persistente
Classicamente l'ipertensione polmonare è definita come un fallimento della normale caduta post-natale delle resistenze vascolari polmonari con conseguente mantenimento degli shunts dx-sn attraverso i canali fetali e quindi ipossiemia.
In molti neonati tali shunts si realizzano a livello intra-polmonare. Tale ipertensione polmonare può essere Primaria, da disfunzione dell'endotelio vasale, con ipossiemia e quadro radiologico polmonare normale, ovvero secondaria ad una patologia del parenchima polmonare, in cui la vasocostrizione è probabilmente secondaria all'ipossia ed all'acidosi.
Il trattamento ventilatorio di questi neonati è spesso controverso. In generale, si imposta una FiO 2 per mantenere una PaO 2 tra 80-97 mmHg al fine di minimizzare la vasocostrizione polmonare; la frequenza ventilatoria e le pressioni devono essere tali da mantenere un pH arterioso di 7,45-7,55. Si evitano PaCO 2 estremamente basse (< 20 mmHg), le quali possono causare vasocostrizione cerebrale. Alcuni neonati si giovano dell'HFOV, mentre NO inalato migliora l'ossigenazione soprattutto nei nati a termine.
Conclusioni
L'introduzione della terapia suppletiva con surfattante e le nuove modalità di assistenza ventilatoria rese possibili grazie ai notevoli sviluppi tecnologici hanno notevolmente ridotto la mortalità e la gravità delle sequele nei neonati prematuri ed a termine con insufficienza respiratoria.
Una conoscenza approfondita dei meccanismi fisiopatologici polmonari, le conoscenze sulla meccanica polmonare e sugli scambi gassosi risultano essere indispensabili al fine di ottimizzare la ventilazione meccanica in questi pazienti.
Infine lo sviluppo di nuove filosofie ventilatorie tendenti a ridurre il danno polmonare ventilatore-indotto unitamente alle numerose modalità alternative di ventilazione potrebbero contribuire ulteriormente a migliorare l'outcome in questi neonati.
Bibliografia
- Bancalari E, Sinclair JC: Mechanical ventilation. In: Sinclair JC, Bracken ME, eds. Effective Care of the Newborn Infant. New York : Oxford University Press; 1992.
- Sinha SK , Donn SM: Advances in neonatal conventional ventilation. Arch Dis Child Fetal Neonatal Ed 1996 Sep; 75(2): F135-40
- Jerreau P.H., Moriette G. et al.: Patient-triggered ventilation decreases the work of breathing in neonates.Am. J. Respir. Crit. Care Med. 1996 Mar.; 153 (3): 1176-81
- Wally C., Bellettato M.: Assisted ventilation of the newborn. www.emedicine.com
- Cleary J.P., Bernstein G. et al.: Improved oxygenation during synchronized intermittent mandatory ventilation in neonates with respiratory distress syndrome: a randomized, crossover study. J. Pediatr. 1995 Mar; 126(3):407-11
- Smith K.M., Wahlig T.M. et al.: Lower respiratory rates without decrease in oxygen consumption during neonatal synchronized intermittent mandatory ventilation. Intensive Care Med. 1997 Apr; 23(4):463-8
- Dimitriou G., Greenough A. et al.: Synchronous intermittent mandatory ventilation modes compared with patient triggered ventilation during weaning. Arch. Dis. Child. Fetal Neonatal Ed. 1995 May; 72(3) FI 88-90
- Carlo WA, Greenough A, Chatburn RL: Advances in conventional mechanical ventilation. In: Boynton BR, Carlo WA, eds. New Therapies for the Neonatal Respiratory Failure. New York : Cambridge University Press; 1994
- G.F. Maffei: CPAP nel neonato: applicazioni e limiti. Italian Internet Journal of Pediatric and Neonatal Anesthesia Anno 2004, Volume 2, N. 1, Gennaio-Febbraio
- G. Rinaldi , G.F. Maffei: il weaning respiratorio nei VLBW. Developmental Physiopathology and clinics. Suppl. Vol.9, 1999, pg.122-128
- Chan V., Greenough A.: Comparison of weaning by patient triggered ventilation or synchronous intermittent mandatory ventilation in preterm infants. Acta Paediatr. 1994 Mar.; 83(3):335-7
- Baumer JH: International randomised controlled trial of patient triggered ventilation in neonatal respiratory distress syndrome. Arch Dis Child Fetal Neonatal Ed 2000 Jan; 82(1): F5-F10
- C. Moretti: I sistemi RC e la costante di tempo. In Disturbi respiratori del neonato. Ed. Masson, 2002, Cap. 7, pg. 107-112